ПРИМЕНЕНИЕ ФЕРРОМАГНИТНЫХ МАТЕРИАЛОВ
ДЛЯ ДИАГНОСТИКИ
И ЛЕЧЕНИЯ ХИРУРГИЧЕСКИХ ЗАБОЛЕВАНИЙ.
Черкасова Ольга Гавриловна 1 , Цыбусов Сергей Николаевич 2 .
1. Московская
медицинская академия имени И. М. Сеченова, Москва, 5 Парковая улица, дом 21, кафедра
аналитической химии. Телефон: 8 – (095) – 165 – 37 – 47.
2. Нижегородская
государственная медицинская академия, Нижний Новгород, 603104, улица Медицинская, дом 1, кафедра
оперативной хирургии и топографической анатомии. Телефон: 8 – (8312) –
65 – 59 – 04. E – mail: Kriol@kis.ru
1. Основные итоги исследований по
созданию магнитных лекарственных средств.
Исследования по
созданию наружных лекарственных средств (МЛС) проводились, в основном, по двум
направлениям: разработке магнитных мазевых
композиций и разработке магнитных ректальных суппозиториев (МРС).
Магнитным
наполнителем мазевых композиций на гидрофильных и гидрофобных основах служил
высокодисперсный магнетит.
Предложены
способы получения магнетитовой пасты-концентрата (МПК), магнитных мазей (ММ) на вазелин-ланолиновой основе (ВЛО) с
метилурацилом (МУ) и диокисдином, магнитных
мазевых основ на базе коллагена и метицеллюлозы (ММО).
Совместимость в
одной лекарственной форме (ЛФ) высокодисперсного магнетита и традиционных
компонентов мазевых композиций доказана методами ИК, УФ, ЯМР-спектроскопии, титриметрии, магнитными и
реологическими измерениями. Выявлены бактерицидные и бактериостатические
свойства МПК, ММ, ММО с высокодисперсным магнетитом (Селезнёв А.С., Литвинова Л. Г.)
Установлено
частичное окисление магнитной фазы композиций с магнетитом на гидрофобных и
гидрофильных основах при получении и хранении. Показано, что в результате окисления образуется твёрдый раствор g-Fe2O3 в магнетите; окисление не сопровождается заметным изменением
намагниченности насыщения образцов с магнетитом. Полученные данные прослужили
основой для разработки критериев оценки качества композиций с магнетитом.
Показана
возможность и целесообразность использования ММ на ВЛО для обтурации наружных
кишечных свищей (Франк В. А.), свищей пищевого
анастомоза (Мамонтов А. С., Решетова И.
В.). МПК использована в новом способе магниторефлексотерапии, исключающем возможность инфекционного заражения (вирусный
гепатит, СПИД). ММ с МУ использована в новом
способе мирингопластики, основанном на
использовании сил магнитного притяжения для фиксации кожного лоскута на
поверхности перфорированной барабанной перепонки (Коченов В. И.), а также применена в новом способе протезирования
глазного яблока, разработанного в МНТК «Микрохирургия глаза» (Линник Е. А., Шлыгин В. В.). В опытах на животных показана
целесообразность использования ММО на метицеллюлозе для очистки гнойных ран.
Второе
направление исследований – создание МРС. Магнитным наполнителем в них служил
феррит бария.
Доказана
совместимость феррита бария с рядом суппозиторных основ (витепсолом, маслом какао, сплавом твёрдого жира и эмульгатора № 1, полиэтиленгликоля) и лекарственных веществ (метилурацилом, пармидином, новокаином).
Предложены способы
получения изотропных и анизотропных МРС без лекарственного вещества, МРС пармидина, МРС новокаина.
Выявлена связь между индукцией на поверхности суппозиториев (BS) с характером их намагниченности и
биологическим эффектом.
Установлено, что МРС без лекарственного вещества (BS = 20 – 25 мТл) показаны при аномальной патологии (острые и
хронические анальные трещины, тромбоз геморроидального узла, анальная форма болезни Крона) без выраженных нарушений функции
кишечника (Григорьева Г. А., Хаммад Е. В.).
Разработаны критерии оценки качества, установлен срок годности МРС без
лекарственного вещества.
Проведён
комплекс физико-химических исследований МРС пармидина. Сформулированы критерии
оценки этой ЛФ. Испытания острой и хронической токсичности, местно-раздражающего действия МРС пармидина
свидетельствуют о том, что при
длительном применении магнитные свечи хорошо переносятся животными, не обладают местно-раздражающим действием, не оказывают отрицательного влияния на кровь и внутренние
органы животных (Саидов Н. Б., Жуков Б. Н,).
Выявлено более выраженное местное противовоспалительное действие МРС пармидина
по сравнению с их традиционным аналогом (Умарова С. А., Саидов Н. Б., Жуков Б. Н., Григорьева Г. А.). МРС пармидина успешно прошли
клинические испытания и разрешены к применению Фармакологическим комитетом.
Разработана
технология продольно- и поперечно-намагниченных МРС новокаина с заданным
значением индукции возле полюсов в интервале 0 – 50 мТл. Магнитооптическая и
биологическая оценка свойств продольно- и
поперечно-намагничивающих свечей свидетельствуют в пользу последних. Показана
возможность снижения массовой доли магнитного наполнителя в свечах при
сохранении значения BS возле полюсов за
счёт модификации промышленного порошка феррита бария марки А дополнительным
отжигом при температуре 950°С, с обработкой поверхности порошка хлороводородной кислотой
и использованием в качестве наполнителя «дроблёнки». Последняя представляет
собой своеобразные анизотропные гранулы, полученные тонким помолом оксидных керамических магнитов.
Установлено, что более выраженное обезболивающее действие новокаина в
МРС по сравнению с традиционным аналогом, сочетается с мягким послабляющим действием этой новой лечебной
формы.
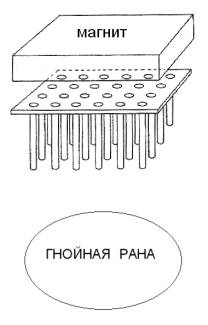
2. Использование магнитной мази при лечении гнойных ран
Лечение гнойных ран остаётся одной из сложных проблем
в хирургии. Увеличение роста антибиотикоустойчивой микрофлоры и осложнённых
форм раневой инфекции заставляет искать новые пути воздействия на местный
иммунитет и регенеративные процессы в ране. Для местного лечения гнойных ран
применяют различные медикаментозные и физические методы – ультразвуковую
обработку, магнито-импульсную терапию и так далее, но ни один из применяемых способов не является достаточно
эффективным. Проведённые исследования о воздействии магнитных полей на течение
раневого процесса с применением ферромагнетиков даёт положительный эффект для
ускорения очищения и заживления раны.
 В результате
многочисленных медико-биологических экспериментов было выявлено, что биологическая среда (лимфа, кровь) разрушает часть полимерного
наполнителя, не касаясь при этом ферромагнитного микрокристалла. В результате
поверхностный слой микрокристалла приобретает большое количество пор, благодаря чему появляется способность сорбировать в них
молекулы токсинов, микроорганизмы, погибшие клетки. Как известно, раны бывают различными по конфигурации, величине, глубине и так
далее и не всегда бывает возможным полностью очистить, то есть удалить ферромагнитную мазь (ФММ) с
продуктами гноя, распада за один приём.
В результате
многочисленных медико-биологических экспериментов было выявлено, что биологическая среда (лимфа, кровь) разрушает часть полимерного
наполнителя, не касаясь при этом ферромагнитного микрокристалла. В результате
поверхностный слой микрокристалла приобретает большое количество пор, благодаря чему появляется способность сорбировать в них
молекулы токсинов, микроорганизмы, погибшие клетки. Как известно, раны бывают различными по конфигурации, величине, глубине и так
далее и не всегда бывает возможным полностью очистить, то есть удалить ферромагнитную мазь (ФММ) с
продуктами гноя, распада за один приём.
Поставленная
задача достигается тем, что при
нанесении ФММ на раневую поверхность, и воздействии
магнитным полем (МП) создаваемым мазью и очистке раны при помощи внешнего
источника постоянного МП, в ране создают
множественные мелкие очаги максимально неоднородного магнитного поля с экспозицией на 1 – 3 минуты.
Под общим
эфирным наркозом у белых беспородных крыс на участке спины наносят кожную рану
до мышцы размером 2 х 2 см. На рану пипеткой наносят 0, 2 мл взвеси стафилококка суточной культуры разведённой до 10 4. Пробы с
поверхности инфицированной раны брали по методу Н. Б. Мордвиновой. После на
рану наносят 0,1 мл ферромагнитной мази. Магнитная мазь представляет собой смесь мазевой основы (ланолин-вазелин) и
высокодисперсный магнетит с размерами кристаллов от 100 до 300 ангстрем со
стабилизатором. При температуре тела
мазь является вязкой, гидрофобной и высоко адгезивной. Намагниченность мази
колеблется в пределах 40 – 60 кА / м. Мазь легко
соединяется с гнойным содержимым. Экспозиция магнитной мази на ране 5 – 7
минут. Рану накрывают салфеткой и подносят кассету, со стальными стержнями и внешним источником ПМП, предварительно сформированную по форме раны, тем самым, создавая в ране максимально неоднородное МП с
выдержкой 1 – 3 минуты.
Пример 1. У
лабораторного животного № 17 в результате очистки предложенным способом
гнойной раны размером 2 х 2 см получено сокращение сроков эпителизации раны на
4 дня по сравнению с контрольной группой.
Пример 2. У
лабораторного животного № 31 в результате двукратной очистки гнойной раны
предложенным способом достигнуто сокращение сроков эпителизации раны по сравнению
с контрольной группой на 5 дней.
Получаемая
высокая неоднородность МП позволяет ориентировать ферромагнитную частицу с обволакивающим
её гнойным содержимым к ближайшему источнику МП, улучшает эвакуацию магнитных частиц, тем самым, обеспечивая
возможность ускорения очистки раны. Бактериостатический эффект обеспечивается
за счёт высокой неоднородности МП. Создаётся дополнительный терапевтический эффект ускорения заживления
раны за счёт упорядоченного множества источников максимально концентрированного
МП. Экспозиция 3 минуты достаточна для очищающего терапевтического воздействия.
3. Мирингопластика с использованием мягких магнитных форм в эксперименте.
Наиболее частыми
причинами отторжения пластического лоскута, если не принимать во внимание варианты наличия тканевой
несовместимости, являются недостатки фиксации
трансплантата на краях деэпителизированной барабанной перепонки. В плоскости
контакта деэпителизированной поверхности и лоскута остаются сгустки крови, препятствующие приживлению в ближайшем послеоперационном
периоде. Могут иметь место воздушные прослойки, ведущие к неполному прилеганию лоскута. Возможно его смещение при
непроизвольных чиханиях, кашле, резких движениях головы. Все эти недостатки ведут к
неприживлению пластического лоскута и безуспешности хирургического
вмешательства по причине плохого качества фиксации пластического лоскута на
завершающем этапе мирингопластики.
Для фиксации
пластических лоскутов обычно используют введение в наружный слуховой проход
ватных шариков, пропитанных антисептическими
мазями в виде сплошного тампона, заполняющего весь слуховой проход. При этом
качественное и достаточно равномерное прижатие и фиксация лоскута достигаются
только при виртуозных индивидуальных способностях хирурга и наличии большого
клинического опыта. Наряду с этим, наружный слуховой проход остаётся
закрытым после операции в течение 14 – 21 дней, из-за чего невозможно проконтролировать ход регенерации, осуществить перевязки с антисептическими воздействиями в
операционном поле.
Мы впервые применили новый способ мирингопластики, при котором не
требуется введение в наружный слуховой проход тампонов для фиксации
пластического лоскута. Способ основан на использовании сил магнитного
притяжения для фиксации лоскута на поверхности перфорированной барабанной
перепонки и стимуляции регенерации, как магнитным полем, так и лекарственными препаратами. Для этого использовали
магнитную 5 % - ную метилурациловую мазь на вазелин-ланолиновой основе (ФММ).
Для придания мази магнитных свойств в её состав вводили высокодисперсный
магнетит (размер частиц порядка 100 ангстрем). При температуре тела мазь
становилась вязкой, клейкой, гидрофобной и в то же время высокоадгезивной. Намагниченность
данной мази колебалась в пределах 40 – 60 кА / м.
Методика
заключалсь в том, что после деэпителизации краёв
перфорации, гемостаза, через
перфорацию на край внутренней поверхности «membrana tympani» накладывался слой ферромагнитной мази. Затем укладывался
пластический лоскут. Он фиксировался путём размещения в зоне проекции
магнитной мази кольца из тефлона с включёнными в него самарий-кобальтовыми
магнитами.
Были проведены
математические расчёты необходимых магнитных свойств ММФ для достижения
достаточной плотности прилегания протеза к краям перфорации. С этой целью использовались
параметры самарий-кобальтового магнита диаметром 6 мм и толщиной 1,5 мм. При изучении зависимости силы притяжения от массы мази
оказалось, что уже при массе мази 0,3 – 1,0 сила превышает 200 мгс. При этом при
переходе к магнитам меньших размеров (диаметром 1мм и высотой 0,7 мм), как показывали
результаты расчётов, сила должна возрастать, так как увеличивалась напряжённость поля вблизи магнита и
её градиент. Но цифры 200 мгс с запасом достаточно для того, чтобы обеспечить притяжение (для её получения достаточно
нанести 0,3 мг мази). Нанести меньшее
количество мази не удавалось технически. В самом деле, масса мази не превышала 1 мг, масса магнита с указанными параметрами – 5 мг, масса кожного лоскута равна 10 мг. Если использовать два
магнита, то сила притяжения составит не менее
400 мгс, а масса всей системы (мазь, лоскут, магниты) составит
не более 22 мг. Таким образом, указанная
система способна выдержать без отрыва ускорение порядка 18 ускорений
свободного падения, чего более чем достаточно для
успешного достижения поставленной цели.
Такая методика
фиксации пластического лоскута при мирингопластике обеспечивает нежное
постоянное и одновременно надёжное прижатие приживляемых элементов друг к другу, отсутствие в плоскости контакта крови или воздуха, к тому же не требуется применение тампона в наружном
слуховом проходе. Последний остаётся открытым, следовательно, в послеоперационном периоде с первого же дня
можно осматривать лоскут, в первые часы
после операции корригировать его положение, воздействовать на операционную зону, используя стимулирующие регенерацию физиотерапевтические
процедуры.
Всего проведено
53 эксперимента на 18 морских свинках (35 экспериментов) и 9 кроликах (18
экспериментов). Первая серия опытов на морских свинках заключалась в ведении
ферромагнитной мази в среднее ухо, наблюдении за
состоянием его после подобного вмешательства. Анестезия обеспечивалась
внутрибрюшинным дробным введением тиопентала натрия. При отомикроскопии
(использовался операционный ЛОР-микроскоп) иглой производилась перфорация
барабанной перепонки, через образовавшийся дефект
механическим шприцем вводилось 0,1 мл ФММ. В течение 2 – 7 – 14 суток после
отомикроскопического контроля животные выводились из эксперимента, осуществлялся забор органов и тканей для гистологического
исследования. При контрольном исследовании обнаружено, что в большинстве случаев в ответ на травму барабанной перепонки
и введение ФММ в среднее ухо развивался негнойный реактивный средний отит. В то
же время на 7-е сутки эксперимента мази в барабанной полости не определялось, что свидетельствовало о её эвакуации через евстахиеву
трубу и перфорацию. На основании данных макро- и микроскопических исследований
был сделан вывод о том, что применение
ферромагнитной мази в хирургической и ототерапевтической практике возможно
(ФММ в свободном состоянии не задерживается в полости среднего уха, ферромагнитная мазь при нанесении её на барабанную
перепонку и на слуховую трубу оказывает противовоспалительный эффект).
Однако на
морских свинках, по ряду морфофизиологических
особенностей их ЛОР-органов, невозможно в
достоверной мере смоделировать процесс ферромагнитной мирингопластики. Поэтому
дальнейшие эксперименты выполнялась на кроликах и включали в себя введение ФММ
с последующим установлением в наружный слуховой проход частиц самарий-кобальтового
магнита: после деэпителизации и подготовки ложа магнитную
мазь специальным микроинструментом точечно наносили на внутреннюю поверхность
барабанной перепонки по периметру перфорации. Затем укладывали пластический
лоскут на полость барабанной перепонки по обычной методике. Для фиксации
пластического лоскута на его поверхность ставили кусочки самарий-кобальтового
магнита размерами до 1 – 3 мм. Они сами притягивались к зоне расположения
магнитной мази под барабанной перепонкой. Таким приёмом достигалось плотное
прилегание лоскута к подготовленной поверхности. Сила прижатия была равномерной
и постоянной, даже довольно резкие движения головой не приводили к смещению
магнитов и лоскута.
Кусочки магнита снимались с пластического лоскута в зависимости от интенсивности регенерации на 7 – 10 день. К этому моменту отмечалось плотное прилегание и надёжное приживление лоскута по краям перфорации. Мазь размагничивалась и начинала проявлять свойства текучести и удалялась естественным путём из барабанной полости через слуховую трубу.
В ходе
экспериментов получены следующие результаты:
1. ФММ удерживается
в барабанной полости только в присутствии магнита, при удалении последнего мазь свободно выводится через слуховую
трубу.
2. При введении ФММ
в барабанную полость и размещении магнита на барабанной перепонке наблюдались
небольшие реактивные изменения окружающих тканей, которые купировались самостоятельно.
3. ФММ при
нанесении её на воспалённую слизистую оболочку оказывает определённый
антибактериальный эффект. При контрольных осмотрах отмечалось уменьшение выделений
из уха, стихание воспалительных явлений.
4. При удалении
кусочков магнитов, ФММ самостоятельно удаляется
через слуховую трубу в течение 7 – 14 дней.
5. В отдалённом
периоде (срок 30 – 45 дней) воспалительные явления в среднем ухе и наружном
слуховом проходе не отмечались.
Полученные результаты позволяют приступить к широкому и успешному применению данного метода в клинической работе.
4. Магнитоуправляемая гемосорбция
Одним из путей оптимизации существующих методов экстракорпоральной детоксикации организма является поиск принципиально новых подходов к реализации идеи гемосорбции.
В это плане
перспективным направлением является разработка магнитоуправляемой детоксикации
организма с применением магниточувствительных сорбентов.
Мы попытались
разработать новую концепцию гемосорбции, которая позволяла бы смягчить или полностью устранить недостатки
традиционных методик.
Предлагаемый
нами метод экстракорпоральной детоксикации организма основывается на введении в
кровь дисперсных ферромагнитных композиций, обладающих соответствующими адсорбирующими свойствами и
дальнейшей сепарации их в магнитной ловушке.
Нами был
разработан и выполнен аппарат для осуществления магнимтоуправляемой гемосорбции.
Получен жидкий магниточувствительный сорбент с размером гранул от 10 до 100 мкм, состоящих из трёх основных компонентов:
1.
Матрицы сетчато-волокнистой структуры из гемосовместимого
материала (в нашем случае из поливинилового спирта);
2. Ферромагнитного
ядра (магнетит);
3. Собственно
сорбента, в качестве которого
использовались как промышленные угольные гемосорбенты, аниониты, а ткаже фермент
- ацетилхолинэстераза как специфический
рецептор к фосфороорганическим соединениям.
Установка
и серия сорбентов были изучены в стендовых экспериментах и в сотрых опытах на
животных. В результате проведённых исследований были сделаны следующие
заключения:
1.
Устройство для осуществления магнитоуправляемой гемосорбции должно
состоять из блока ввода магниточувствительного сорбента, смесителя, магнитного
сепаратора, воздушной ловушки, блока контроля за качеством сепарации и переходных трубок;
2.
Метод эмульсионной полимеризации позволяет получать
магниточувствительные сорбенты с различными свойствами и диаметром гранул от
10 до 150 мкм;
3.
Использование в качестве сорбционной составляющей нового
детоксиканта (размолотого ионита АВ-17-8) позволяет повысить эффективность
связывания билирубина в 3 раза;
4.
Внутривенное введение высокодисперсного синтетического магнетита в
дозе до 100 мг / кг не приводит к значительным
изменениям в свёртывающе-антисвёртывающей системе крови. Применение большей
дозы вызывает развитие синдрома диссеминированного внутрисосудистого
свёртывания крови.
Химическое «подшивание» к дисперсному магниточувствительному носителю ферментов возможно и позволяет осуществлять высокоселективное связывание патогенных метаболитов. Этот факт доказывает эффективность использования экстракорпоральной магнитоуправляемой гемосорбции при острых отравлениях фосфороорганическими веществами в эксперименте.
5.
Ферромагнитная иглорефлексотерапия
В настоящее время общепризнанно
положительное влияние магнитного поля малой индукции на организм человека, как и
методов рефлексотерапии. Поэтому мы попытались соединить два подхода и создать
пунктурную магнитотерапию.
В своей работе мы
преследовали следующую цель: осуществить концентрацию
магнитной энергии в нескольких биологически активных точках (то есть
сформировать «Магнитные иглы»), исключив при этом
возможность инфекционного заражения, болевые и другие субъективно
неприятные ощущения.
Для этого было разработано
устройство, представляющее собой источник поля и
несколько выносных концентраторов магнитной энергии. Последние представляют
собой комплексдвух полусфер: внутренней – диамагнитной, и наружной – ферромагнитной, выполненной
из ненамагниченной мягкой густой магнетитовой мази на вазелин-ланолиновой
основе с величиной намагниченности насыщения 75 – 80 кА/м. Концентраторы имеют размеры
от 3 до 5 мм и легко наносятся на биологически активные точки посредством специального
устройства.
Данный способ и устройство
позволяют менять интенсивность и глубину проникновения поля в зависимости от
индивидуальной реакции и клинических потребностей. При воздействии внешним
магнитным полем появляется возможность проводить параллельно к магнитоаккумпунктуре
магнитотерапию облучаемой зоны. В результате этого лечебный эффект возрастает
на 25 – 30 %.
Предлагаемый способ и
устройство применены в условиях больницы № 33 Нижнего Новгорода у 21 пациента
с различными заболеваниями.
Больные с гипертонической
болезнью после 3 – 4 процедур наблюдали значительное улучшение общего
самочувствия, исчезновение головных болей, головокружений,
нормализацию сна, снижение артериального давления. К концу курса
лечения отмечали закрепление выше перечисленных эффектов,
снижение артериального давления в среднем на 10 – 20 мм ртутного столба и его
стабилизацию, положительные сдвиги в ЭКГ (смена брадикардии на
нормокардию).
В группе больных с
патологией опорно-двигательного аппарата уменьшение болей в области суставов
наблюдали со 2 процедуры, полное исчезновение
болевого синдрома отмечали к 8 процедуре. К концу курса лечения происходило
полное исчезновение болей и восстановление полного объёма движений в
поражённом участке.
Таким образом, устройство,
созданное на основе магнетитовой мази и новый способ магниторефлексотерапии
позволяют сконцентрировать магнитную энергию в форме «магнитных игл»
одновременно в нескольких местах, применять различные виды
магнитного и электромагнитного полей для лечения различных видов патологии,
исключить риск инфекционного заражения пациентов, болевых и субъективных
неприятных ощущений при выполнении процедур. При этом сохраняется высокая
эффективность проводимой терапии.
6. Использование ММЛФ в криохирургии и криотерапии нёбных миндалин.
Хронический
тонзиллит проджолжает лидировать в структуре патологии ЛОР органов. В его
лечении в последние годы произошёл поворот в сторону щадящего отношения к
иммунокомпетентному органу – небным миндалинам, в сторону использования
щадящих, стимулирующих, противовоспалительных и регенеративных методик [4, 5].
В силу того, что в зависимости от способа воздействия криогенные методы
лечения могут вызвать различные эффекты от иммуностимуляции, стимуляции регенеративных процессов, до полной деструкции ткани, криогенные воздействия являются самыми перспективными
универсальными методами лечения [1, 7].
Активное
совершенствование техники традиционных лучевого и химиотерапевтического лечения
опухолевых заболеваний нёбных миндалин не привело к существенному улучшению
его эффективности. Это выводит на первый план
криогенные методы лечения. Ведь криогенное разрушение является наиболее
адекватным и физиологичным лечебным приёмом и может применяться как
самостоятельно, так и в сочетании с лучевыми и химиотерапевтическими воздействиями.
Известны два варианта локального охлаждения тканей с
лечебной целью: криоорошение – воздействие непосредственно струёй жидкого азота и
аппликационный, когда на ткань воздействуют
охлаждённой поверхностью криоинструмента, а жидкий азот циркулирует внутри его.
Из-за
особенностей локализации миндалин, криоорошение
при их лечении затруднительно и травматично. Наиболее широко используется
аппликационный метод криовоздействия [8, 11,
12].
Созданы
различные формы аппликаторов и наконечников инструментов, адаптированные к конкретным анатомическим условиям глотки [13, 14]. Однако, во всех случаях открытой остаётся проблема создания плотного
механического и теплового контакта поверхности аппликатора и миндалин. Без
этого не удаётся достаточно эффективно отводить тепло из глубины ткани [6]. Криодеструкция бугристых поверхностей, какими и являются нёбные миндалины, неровных опухолевых патологических образований оказывается
часто затруднительной.
В существующих
подходах и методиках криогенного терапевтического и хирургического лечения
нёбных миндалин остаётся много проблем и недостатков. Так, например, при проведении
иммуностимулирующей криотерапии на поверхности нёбных миндалин, не осуществляется охлаждение непосредственно внутри
лакун. Образующийся после замораживания на поверхности миндалин фибринозный
налёт закрывает крипты. Присутствующие в них гноеродные микроорганизмы
зачастую вызывают ангиноподобную реакцию, обострение тонзиллита, с резким
подъёмом температуры. Это серьёзные нежелательные осложнения, ведь речь идёт о терапевтической методике [8].
При проведении криотонзиллотомии несоответствия
поверхности миндалин и плоскости аппликатора не дают возможности быстро и
эффективно провести глубокое локальное замораживание ткани миндалин или
находящейся в ней опухоли.
В настоящее время пристальное внимание исследователей
новых лечебных методов в различных клинических областях привлекает недавно
разработанный вид лекарственных средств – мягкие магнитные лекарственные формы
(ММЛФ).
Ценность ММЛФ для криологии мы увидели в том, что они имеют
очень высокую теплопроводность, сравнимую со
сплошным металлическим объектом, причём
теплопроводность всех мягких магнитных лекарственных форм резко возрастает при
наличии внешнего постоянного магнитного поля [2].
Примечательно, что в магнитном поле мягкая ферромагнитная лекарственная
форма сама намагничивается, выполняя роль
противоположного полюса магнита, а между двумя
магнитами – роль сердечника. При этом частички железа внутри мази
выстраиваются в цепочки в соответствии с направлением линий напряжённости
магнитного поля. Вытянутые в линии частички железа вступают в контакт друг с
другом, именно поэтому под воздействием
магнитного поля теплопроводность ферромагнитной лекарственной формы
увеличивается [3].
Кроме этого, ММЛФ даёт противовоспалительный, стимулирующий регенерацию эффект, характеризуется выраженным высушивающим раневую поверхность
действием [3]. А крионекроз обычно оказывается
в первые дни после его появления влажным, и находится долго на месте, пока происходит регенерация под ним нового эпителия.
Мы впервые
использовали эти особенности ММЛФ в практической криологии. ММЛФ применена
нами в качестве теплопередающей прослойки между криоаппликатором и биологической
тканью, в частности, при лечении нёбных миндалин.
С
терапевтической целью было пролечено более 50 больных с хроническим тонзиллитом, иммунодефицитными состояниями. Криотерапия при хроническом
тонзиллите не была направлена на разрушение функционально ценной
иммунокомпетентной ткани нёбных миндалин, поэтому подачу жидкого азота с промежутками включали, буквально, на несколько секунд
многократно.
Суть методики
заключалась в следующем. У больных
хроническим тонзиллитом крипты нёбных миндалин предварительно тщательно
освобождали от пробок промыванием их антисептиками с перекисью водорода. Мягкую
ферромагнитную лекарственную форму наносили на поверхность миндалин. С
противоположной стороны, из подчелюстной области, воздействолвали полем постоянного самарий-кобальтового магнита
или электромагнита. При этом изменяли в небольших пределах направленность и
напряжённость магнитного поля. Для этого магнит медленно перемещали в
пространстве. При подобных манипуляциях создавались изменения направленности и
силы магнитного притяжения мягкой ферромагнитной лекарственной формы. Мягкая
или жидкая ферромагнитная форма, под действием
внешнего магнитного поля, погружалась, насколько это
возможно, в трещинки и щели, заходила в открытые с поверхности полости и каналы в
глубине ткани, при этом ферромагнетик входил в
крипты через лакуны нёбных миндалин. В результате этого создавались теплопроводящие
каналы в тех участках патологической ткани, которые без этого были бы препятствием для прохождения холода в
глубину патологической ткани.
Замораживание
проводили не прекращая воздействие магнитного поля. Было отмечено, что несмотря на отсутствие прилипания
криоинструмента к ткани, имеющее место при использовании мазей в первый момент
криовоздействия до отвердевания мазевой основы, воздействие не было сопряжено с плохой теплопроводностью, так как теплопроводность насыщенной магнетитом мази, находящейся в магнитном поле, со строго ориентированными по магнитным линиям частичками
металла, существенно не отличается в разных
агрегатных состояниях – мягком и твёрдом.
Сначала объёмный
магнит размещали в подчелюстной области и за углом нижней челюсти, после этого через специальную канюлю в лакуны нёбной
миндалины вводили под местной анестезией (для снятия рвотного рефлекса) 0,5 – 1,0 мг ММЛФ с добавлениями сосудосуживающих
и антисептических средств. За счёт воздействия магнитного поля и перемещений
магнита в пространстве ММЛФ распределялась в криптах, которые взаимосвязаны между собой. Затем, вводили дополнительно по небольшой порции ММЛФ в каждую лакуну.
Слой ММЛФ дополнительно наносили на поверхность аппликатора, приводили его в контакт с поверхностью миндалины. При
этом вся ММЛФ собиралась в единое целое в магнитном поле.
Начинали охлаждение аппликатором за счёт циркуляции в
нём жидкого азота. ММЛФ, имея существенно лучшую теплопроводность, чем кровоснабжённая ткань миндалины, обеспечивала охлаждение лимфоидной ткани не только на
поверхности, но и в лакунах и криптах нёбных
миндалин.
У всех больных
отмечен отличный криотерапевтический эффект, ангины больше не повторялись. После воздействия не было отёка и
местной реакции нёбных дужек. Отмечено выраженное общеоздоравливающее, иммуностимулирующее действие криомагнитной терапии –
прекращались простуды, улучшалось
общее самочувствие.
В послеоперационном периоде несколько дней наносили на
поверхность миндалин ферромагнитный гель, содержащий антисептик, анестетики,
сосудосуживающие препараты димексид, метилурацил, иногда антибиотики и воздействовали внешним магнитным
полем.
Мы впервые
начали использование ММЛФ в ходе криогенных
хирургических магнипуляций. В частности, при криохирургическом лечении гипертрофического тонзиллита (5
пациентов) и опухолевых образований нёбных миндалин (у 2 больных с опухолью
Шминке).
Методика лечения
отличалась от воздействий с терапевтической целью большей экспозицией
криовоздействий (до 3 – 4 минут) и соответственно большими размерами зоны
замораживания и крионекроза.
Отмечено
увеличение скорости охлаждения опухолей на 25 – 30 %, сохранение активной теплопередачи после достижения аппликатором
уровня температуры ниже – 120 °С. Уменьшение отёчных
перифокальных изменений и отторжения крионекроза, полного заживления уменьшились по сравнению с обычными при таких
же объёмах крионекроза почти в два раза и составили 14 – 20 дней. Осложнений не
отмечено.
Практическое
применение способа и устройства показало целый ряд преимуществ новой методики
и устройства по сравнению с известными приёмами и инструментами.
Предлагаемый
способ позволяет существенно улучшить результаты криохирургического лечения
воспалительных и опухолевых очагов нёбных миндалин за счёт того, что позволял:
1. Во всех
вариантах применения создать более плотный тепловой контакт инструмента с
тканью нёбных миндалин.
2. Ускорить
охлаждение, увеличить его глубину, за счёт этого увеличить повреждающий эффект холода, сократить время охлаждения при операции.
3. Увеличить
криоповреждение за счёт модификации разрушающего эффекта магнитным полем.
4. Способ и
устройство дают возможность увеличить интенсивность проникновения холода в
глубину тканей за счёт вхождения теплопроводного мягкого магнетита в углубления
и каналы в толщу миндалин
5. Не было
временного закрытия лакун крионекрозом, поэтому не было
воспаления и рубцевания в лакунах.
6. Метод позволял
замораживать миндалины любой выпуклости, плотности и бугристости.
7. Облегчилось
ведение послеоперационного периода.
8. Осуществление
способа позволило почти в два раза быстрее высушивать крионекроз, ускорять его отторжение, уменьшить его отёчность, экссудацию и
боль.
9. Осуществление
методики не требовало дополнительных затрат, она доступна всем врачам, устройство и мягкие магнитные лекарственные вещества
изготавливались по известным технологиям.
Считаем, что описанные криомагнитные методики разрушения патологических
тканей и противовоспалительного воздействия с локальным охлаждением в магнитном поле через слой ММЛФ и
послеоперационное лечение крионекрозов ММЛФ найдёт широкое практическое
использование в медицине, так как
позволяет улучшить результаты криогенного лечения практически по всем
показателям.
Библиографический список:
1.
Ablin R. J., Soanes W. A., Gonder
M. J. Prospect for cryo-immunotherapy in cases of metastasizing carcinoma of
the prostate Cryobiology, 1971, № 8, P. 271 – 279.
2.
Ахалая М. Г. // Четвёртая
всесоюзная конференция по применению магнитных жидкостей, Сухуми, 1991, С. 9 – 10.
3.
Ахалая М. Г., Вольтер Е. Р., Какиашвили М. С. Дегидратационные свойства коллоидного
магнетита // Четвёртая всесоюзная конференция
по применению магнитных жидкостей, Сухуми, 1991, С. 11 – 12.
4.
Баранов А. Ю., Кидалов В. Н.
Лечение холодом. Криомедицина. Санкт – Петербург, 1999, 272 с.
5.
Дорохов С. Д. Регенеративная криотерапия // В книге: Медицинская криология. Сборник
научных трудов. Нижний Новгород, 2001, C. 69 – 72.
6.
Коченов В. И. Адгезивный эффект в криохирургии // Рукопись депонированная во ВНИИМИ № Д-5061. Реферат в МРЖ, Т. IV, 1982, № 8.
7.
Коченов В. И. Криохирургическая профилактическая онкология. Нижний
Новгород, 2000, 56 с.
8.
Коченов В. И. Криотерапия горла и носа. // В книге: Медицинская криология. Сборник
научных трудов. Нижний Новгород, 2001, C. 94.
9.
Потапов И. И., Рудня П. Г., Тарлычева Л. С., Шеврыгин Б. В.
Криохирургия в оториноларингологии, Москва, 1975.
10. Рылкин А. И., Коченов В. И.
Криотерапия у больных хроническим тонзиллитом // Тезисы докладов V Всероссийского съезда оториноларингологов, Ижевск, 1989, С. 116 – 117.
11. Шахов В. Ю., Рылкин А. И., Коченов В. И. Отдалённые результаты криогенного лечения больных
хроническим тонзиллитом // Рукопись, депонированная во ВНИИМИ, МРЖ, раздел XIII, 1981, № 12, публикация 1323.
12. Шахов В. Ю., Рылкин А. И., Коченов В. И. Отдалённые результаты криогенного лечения больных
хроническим тонзиллитом // В книге: Клиника, диагностика и
лечение воспалительных заболеваний верхних дыхательных путей. Москва, 1982, С. 98 – 100.
13. Шахов В. Ю., Рылкин А. И., Коченов В. И. Устройство
для воздействия на язычную миндалину. //
Авторское свидетельство № 1568998.
14. Шахов В. Ю., Рылкин А. И., Коченов В. И. Устройство для воздействия на
нёбные миндалины // Авторское свидетельство №
1142115.
7. Стандартизация магнитных лекарственных форм.
Разработанные
нами магнитные лекарственные формы (МЛФ) можно условно поделить на две большие
группы:
1.
МЛФ, действие которых, главным образом, основано на силовом взаимодействии с наружным
источником магнитного поля (МП) – это магнетитовая паста-концентрат (МПК), магнитные мази (ММ) без лекарственного вещества (ЛВ), ММ с метилурацилом 5 % и 10 %, ММ с диокисдином 1% [1].
2. МЛФ, которые при введении в организм в течение определённого
промежутка времени выполняют роль локального источника ПМП (постоянного
магнитного поля), оказывая биотропное действие, либо только за счёт МП или за счёт совместного действия МП
и ЛВ. К числу последних относятся магнитные ректальные суппозитории (МРС) без
ЛВ [1 – 4], МРС пармидина (МРСП) [1, 2], МРС новокаина (МРСН) [3], МРС ортофена (МРСО) [4].
В состав МЛФ
первой из выделенных групп входит высокодисперсный магнетит, а в состав второй входит высокодисперсный феррит бария.
Все
перечисленные МЛФ были апробированы в экспериментальных клинических исследованиях
[5] на ограниченном числе волонтёров и
показали свою эффективность и целесообразность применения на практике. Однако
отсутствие нормативно-технической документации, утверждённых методов стандартизации МЛФ препятствует их включению в состав
Фармакопеи, тормозит их широкое применение.
Подготовлен
проект общей фармакопейной статьи на МЛФ. Он включает основные требования к
качеству высокодисперсного магнетита и феррита бария: описание (внешний вид), растворимость, подлинность, количественное
определение, магнитные характеристики, условия хранения.
Определён перечень критериев МРС: твёрдость, масса МРС, температура
плавления, время полной деформации, однородность, качественный
анализ магнитного наполнителя, количественный
анализ магнитного наполнителя,
микробиологическая чистота, максимальное
значение магнитной индукции, условия
хранения, срок годности, фармакологическое действие.
Сформулированы общие указания по критериям и методам контроля качества ММ. Они включают наряду с традиционными критериями качества мазей новый показатель – намагниченность насыщения.
Библиографический список:
1. Черкасова О. Г.
Физико-химические основы применения высокодисперсных магнитных материалов в
фармации. Дисс. … д-ра фармацевтических наук, Москва, 1993, 285 с.
2. Саидов Н. Б.
Феррит бария как компонент магнитных ректальных суппозиториев пармидина. Дис.
… канд. фармацевтических наук, Москва, 1991, 134 с.
3. Денисова М. Н.
Изучение связи между составом и свойствами магнитных ректальных суппозиториев с
ферритом бария. Дис. … канд. фармацевтических наук, Москва, 1997, 126 с.
4. Смолянинова М.
В. Изучение связи между составом и свойствами двухслойных магнитных ректальных
суппозиториев с ферритом бария. Дисс. … кан. Фармацевтических наук, Москва, 2000, 98 с.
5. Цыбусов С. Н.
применение ферромагнитных материалов для диагностики и лечения хирургических
заболеваний. Дисс. д-ра медицинских наук, Нижний Новгород, 1995, 182 с.
Авторы выражают глубокую признательность
Р. Н. Аляутдину, Т. Е. Белоусовой, О. И. Блохину, Г. А. Буланову, С. В. Грачёву, Н. М. Денисовой, С. П. Завадскому, А. А. Игнатьеву, В. И. Коченову, Ю. В. Королёву, Д. Г. Крутогину, И. И. Николаеву, А. Н. Пермичеву, О. А. Савину и Ю. Я. Харитонову за помощь в подготовке материалов к
публикации.